女子美術大学付属中学校理科過去問研究
2021年度女子美術大学付属中学校第1回入学試験は2月1日に実施されました。
第1回入学試験は2科目4科目の選択制で、募集人数105名に対し志願者数362名(2科206名,4科156名) 受験者数354名(2科200名,4科154名) 合格者数120名でした。
第1回科目別合格者平均点は 国語66.4点 算数73.0点 社会38.6点 理科39.1点でした。
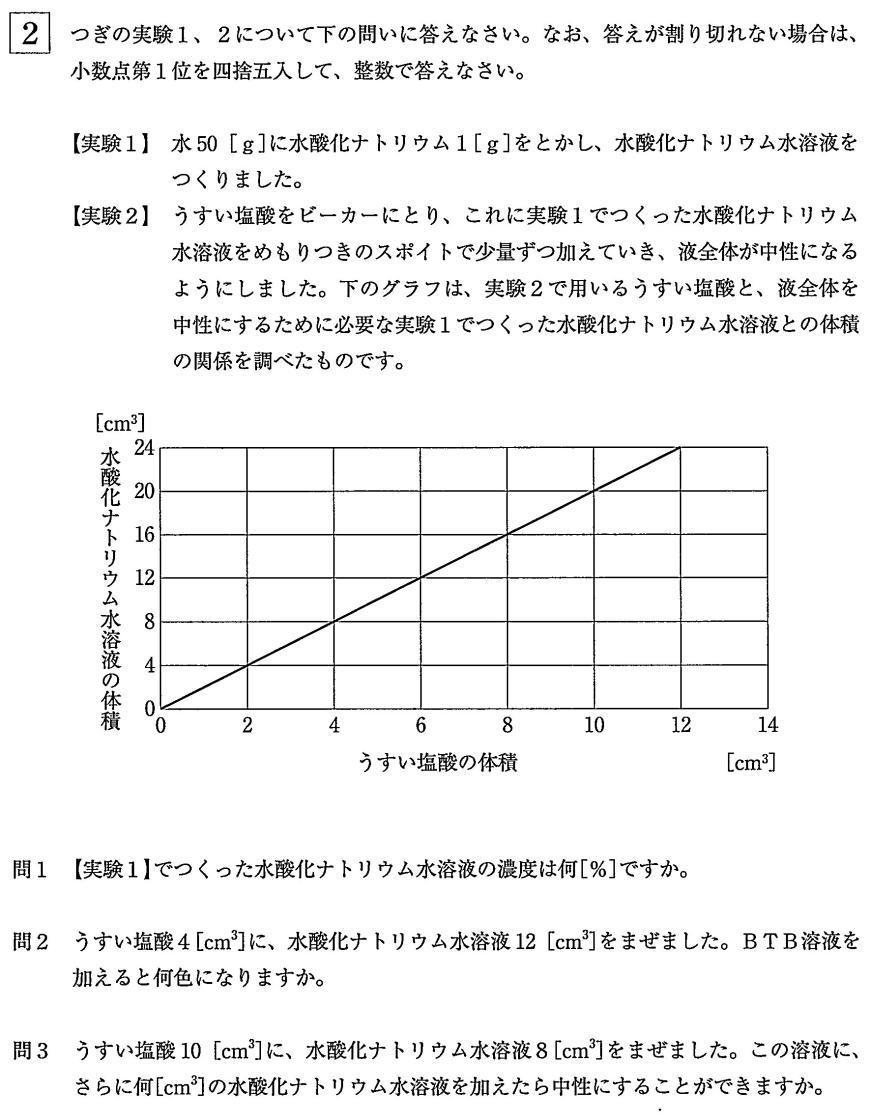
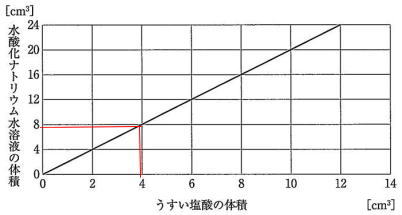
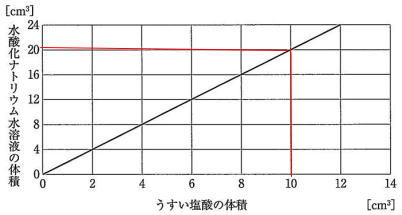
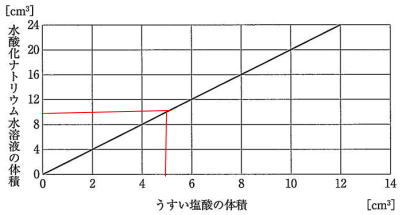
今回は 理科入試問題から2.水溶液の性質を解説します。
知識以外に計算を必要とする出題があります。算数の濃度の計算を利用して解きましょう。