普連土学園中学校理科出題傾向は学校側の説明によると、「小学校の教科書を中心にさらに発展した問題について、物理・化学・生物・地学の各分野からほぼ均等に出題します。グラフや表の読み取りが出題されることが多く、文章での解答を求める問題も必ず出題します。なお、1日午前4科と4日午前4科で、出題方針や問題の水準に違いはありません。」
2021年度普連土学園中学校4日午前4科理科入試問題は、物理・化学・生物・地学からそれぞれ大問1題ずつの出題で、1.物のつり合い 2.化学反応実験 3.インゲンの種子と発芽実験 4.地球の環境と月の動きでした。今回は2.化学反応実験を解説します。
普連土学園中学校2021年度4日午前4科理科入試問題2.二酸化炭素の性質と化学反応実験 問題
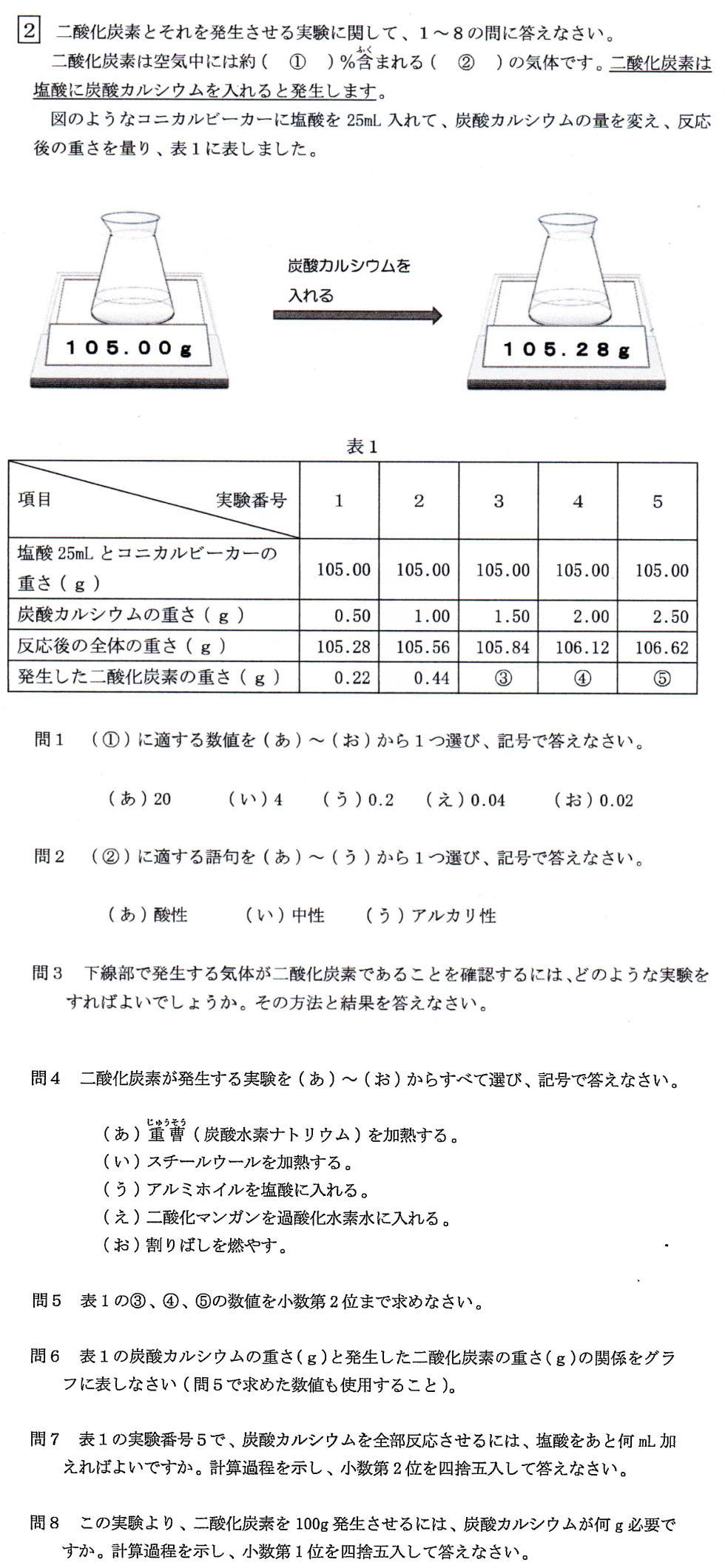
普連土学園中学校2021年度4日午前4科理科入試問題2.化学反応実験 問1 問2解説解答
(あ) 20 (い) 4 (う) 0.2 (え) 0.04 (お) 0.02
問2( ②)に適する数値を(あ)~(う)から1つ選び、記号で答えなさい。
(あ) 酸性 (い) 中性 (う) アルカリ性
解説解答
二酸化炭素は空気中には約(①)% 含まれる(②)の気体です。
二酸化炭素の気体は炭酸ガス、個体はドライアイス、液体は液体二酸化炭素、水溶液は炭酸や炭酸水と呼ばれている。常温では無色無臭の液体。-79℃で昇華して個体(ドライアイス)となる。
大きな圧力を加えるか水の温度を極端に下げると水に溶けやすくなる。それ以外では水に溶けにくい。
水溶液は弱酸性を示す。
答 問1 (え) 問2 (あ)
普連土学園中学校2021年度4日午前4科理科入試問題2.化学反応実験 問3 解説解答
解説解答
二酸化炭素は塩酸に炭酸カルシウムを入れると発生します。
反応式は 炭酸カルシウム + 塩酸 → 塩化カルシウム + 二酸化炭素 + 水
二酸化炭素の性質は 1.空気より密度が大きく、約1.53倍。 2.無色無臭 3.石灰水を白く濁らせる。 4.大きな圧力を加えるか水の温度を極端に下げると水に溶けやすくなる。それ以外では水に溶けにくい。
解答
実験の方法:気体を石灰水に通す。 結果:石灰水が白く濁る。
普連土学園中学校2021年度4日午前4科理科入試問題2.化学反応実験 問4 解説解答
問4 二酸化炭素が発生する実験を(あ)~(お)からすべて選び、記号で答えなさい。
解説解答
(あ) 重曹(炭酸水素ナトリウム)を加熱する。
炭酸水素ナトリウム → 炭酸ナトリウム + 二酸化炭素 + 水
(い) スチールウールを加熱する。
鉄 + 酸素 → 酸化鉄
(う) アルミホイルを塩酸に入れる。
アルミニウム + 塩酸 → 塩化アルミニウム + 水素
(え) 二酸化マンガンを過酸化水素水に入れる。
過酸化水素水 → 水 + 酸素
二酸化マンガンは触媒なので化学反応そのものには直接かかわらない。
(お) 割りばしを燃やす。
炭素 + 酸素 →二酸化炭素
木は主にセルロースという物質でできていて、セルロースの脱水反応がおこり二酸化炭素が生成される。
化学反応式より 二酸化炭素が発生するのは (あ)と(お)
答 (あ)と(お)
普連土学園中学校2021年度4日午前4科理科入試問題2.化学反応実験 問5 解説解答
問5 表1の③,④,⑤の数値を小数第2位まで求めなさい。
解説解答
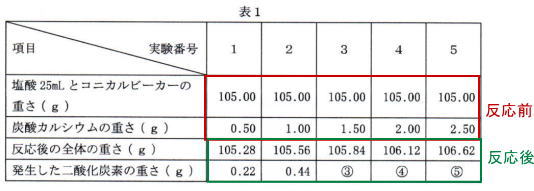
反応前の物質の重さの和と反応後物質の重さの和は等しいので、
③ 105.00 + 1.50 = 105.84 + ③ ③ = 105.00 + 1.50 – 105.84 = 0.66
④ 105.00 + 2.00 = 106.12 + ④ ④ = 105.00 + 2.00 – 106.12 = 0.88
⑤ 105.00 + 2.50 = 106.62 + ⑤ ⑤ = 105.00 + 2.50 – 106.62 = 0.88
答 ③ 0.66 ④ 0.88 ⑤ 0.88
普連土学園中学校2021年度4日午前4科理科入試問題2.化学反応実験 問6 解説解答
表1の炭酸カルシウムの重さ(G)と発生した二酸化炭素の重さ(g)の関係をグラフで表しなさい。
解説解答
省略
普連土学園中学校2021年度4日午前4科理科入試問題2.化学反応実験 問7 解説解答
問7 表1の実験番号5で炭酸カルシムを全部反応させるには、塩酸をあと何ml加えればよいですか。計算過程を示し、小数第2位を四捨五入して答えなさい。
解説解答
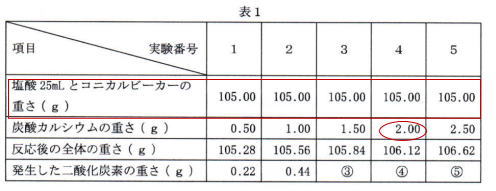
表1実験1~4より塩酸25mlに対して発生する二酸化炭素の重さは炭酸カルシウムの重さと比例しているが、実験5では発生する二酸化炭素の重さは比例していないので、実験4より塩酸25mlに対して炭酸カルシムが反応する最大の重さは2.00g。
塩酸25mlに対して炭酸カルシウムが反応する重さは 2.00gなので、炭酸カルシム1.00gあたり塩酸25÷2=12.5gが必要となる。
よって炭酸カルシウム2.50gが全部反応するのに必要な塩酸の量は 12.5×2.5 = 31.25g
したがって あと 31.25 – 25 = 6.25g必要となる。
答
25÷2×2.5 – 25 =6.25
6.3ml
普連土学園中学校2021年度4日午前4科理科入試問題2.化学反応実験 問8 解説解答
問8 この実験より、二酸化炭素を100g発生させるには、炭酸カルシウムが何g必要ですか。計算過程を示し、小数第1位を四捨五入して答えなさい。
解説解答
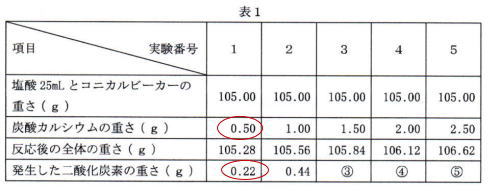
炭酸カルシム0.50gに対して発生した二酸化炭素の重さは0.22g
よって 二酸化炭素1g発生させるのに必要な炭酸カルシムの重さは (0.55÷0.22)g
よって二酸化炭素を100g発生させるのに必要な炭酸カルシウムは 0.55÷0.22×100 = 227.2・・・
答
0.55÷0.22×100 = 227.2・・
227g
